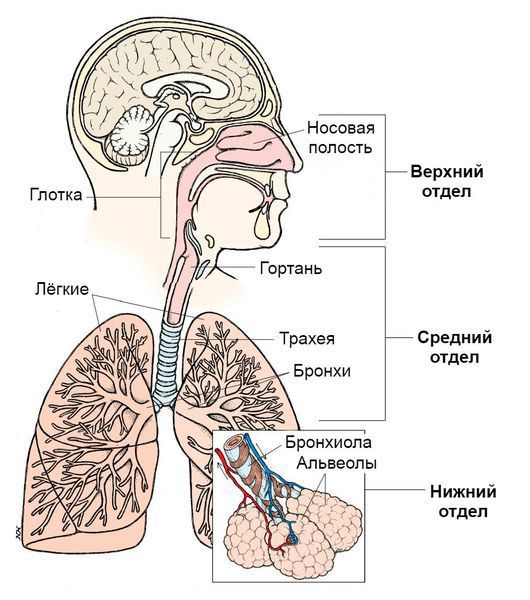
Суть вакцины от коронавируса covid-19: все что нужно знать
Содержание:
- Антител может не быть после болезни. Как тогда поможет вакцина?
- Вакцину уже производят
- Вакцина от коронавируса инст. Чумакова
- Разработка вакцин против COVID-19: логистика
- Где и когда будут производить вакцину «Спутник V»?
- Кто еще в списке?
- Впереди планеты всей
- Почему требуется так много времени для разработки вакцины?
- Вакцина от коронавируса в Германии
- Какие могут быть побочные эффекты у вакцины «Спутник V», какие риски и противопоказания?
- Какие виды вакцин существуют?
Антител может не быть после болезни. Как тогда поможет вакцина?
После перенесенной инфекции или прививки остаются антитела. Их концентрация со временем снижается. В конце концов антитела могут исчезнуть вовсе. Но это не значит, что организм будет беззащитен перед инфекцией. не ограничивается лишь тем, что у переболевшего или привитого вырабатываются специфические антитела. Иммунный ответ — это также и активация B- и T-клеток памяти, которые становятся специфичными для определенной инфекции. Если в ответ на инфекцию или прививку выработался клеточный иммунитет, то у организма осталась способность вырабатывать антитела. И в этом случае (при наличии клеточного иммунитета) при встрече с инфекцией специфические клетки памяти запускают выработку антител, чтобы побороть инфекцию. Кроме того, один из типов T-клеток, а именно CD8+ T-клетки, сам убивает инфицированные клетки организма.
В резюме , вышедшего в Nature, заявляется следующее: «Недавние сообщения о том, что антитела к SARS-CoV-2 не обнаруживаются в крови после выздоровления от COVID-19, вызвали настороженность. Однако отсутствие специфических антител в крови еще не означает отсутствия иммунологической памяти. Здесь мы обсуждаем актуальные представления об относительном вкладе B- и T-клеток в иммунитет против SARS-CoV-2 и их значение для разработки эффективного лечения и вакцин от COVID-19».
Мы пока не знаем, что именно будет играть роль в предотвращении случаев повторного заражения. Впрочем, в недавнем , опубликованном в Nature, заявляется о длительном Т-клеточном иммунитете к структурному белку (не путать со спайковым белком, о котором речь шла выше).
Структура вирусной частицы SARS-CoV-2:
Spike glycoprotein (S) — спайковый, или шиповидный, гликопротеин S
M-protein — мембранный белок M
Hemagglutinin-esterase dimer (HE) — димер гемагглютинин-эстеразы
Envelope — оболочка
RNA and N protein — РНК- и нуклеокапсидный, или структурный, белок N
E-protein — белок оболочки E
Вакцину уже производят
Одно можно сказать с уверенностью: если ее через две недели, действительно, планируют запустить, значит, производство уже идет полным ходом. В какой-то момент к процессу подключилась частная компания «Р-Фарм».
«Если не прививать детей, мы получим еще одну эпидемию». Педиатр — о вакцинации в период карантина
Совсем обойтись без частного сектора в таком деле государственной важности, как производство вакцины, не получится. У государства нет мощностей, чтобы произвести препарат на всю Россию
Кроме того, разработка вакцин обладает крайне низкой вероятностью успеха. Ведь в разработке лекарств без конца все меняется, выходят новые научные работы — и приходится многое пересматривать. В таком режиме государству работать невозможно, поскольку необходимо постоянно пересогласовывать процесс, вероятность успеха которого менее 10%, поэтому госсектор предпочитает с кем-то разделить риски.
У компании «Р-Фарм», безусловно, есть все компетенции и возможности, чтобы произвести вакцину и сделать это по международным стандартам. Это внушало лично мне некоторый оптимизм, поскольку частные компании имеют международные амбиции и могут сделать процесс разработки более прозрачным и профессиональным. Но в случае с вакциной от COVID-19, как я теперь вижу, роль фармкомпаний оказалась незначительна, проект идет в административном формате.
Вакцина от коронавируса инст. Чумакова
Суть вакцины от коронавиуруса
За основу взят цельный вирус, деактивированный на 99% и неспособный размножаться. В результате иммунитет получает полную формулу, из которой самостоятельно выделяет нужные ему фрагменты для формирования антител.
Отличия
В отличие от других вакцин от коронавируса, здесь за основу берется настоящий вирус, которому химическим путем блокируются способности к размножению. Считается, что такой вариант проще разрабатывается и модифицируется в зависимости от мутации.
Однако все опыты с живыми вирусами считаются потенциально опасными, поскольку невозможно гарантировать потери способность к размножению на 100%. Кроме того, иммунитет формируется на конкретный штамм, поэтому человек остаётся беззащитным перед другими мутациям вируса.
На каком сейчас этапе
На сегодня завершены доклинические испытания, показавшие стойкий иммунитет у лабораторных животных. Теперь препарату предстоит пройти первые клинические исследования. Если тест на добровольцах пройдет успешно, заявка на регистрацию будет направлена в феврале 2021 года. Тогда разработка центра им. Чумакова станет третьей вакциной от коронавируса.
Испытания
Препарат ещё не испытывался на добровольцах. Поэтому данных о побочных действиях нет. Заявка на клинические испытания вакцины Чумакова от коронавируса была направлена 23.08.2020, и в ноябре этого года она была одобрена. По сообщению ТАСС, ожидаемое число участников составит 3 000 человек, которые после вакцинации останутся на 16 дней в стационаре под наблюдением врача.
Разработка вакцин против COVID-19: логистика
Еще одна большая проблема — производство и распространение вакцины. Многие читатели слышали о трудностях, которые иногда возникают в процессе производства вакцины против гриппа, что приводит к ее дефициту. В зависимости от того, какая технология получения вакцин выходит на первое место, производство достаточного количества доз воспроизводимым способом может быть довольно сложной задачей. Кроме того, многие вакцины нуждаются в перевозке и хранении в холодных условиях, что также бывает трудно обеспечить. А что делать, если возможная вакцина требует более одной инъекции, что справедливо, например, для многих вакцин с адъювантами? Отслеживать это — еще одна проблема.
То, чему мы сейчас свидетели — это беспрецедентный вызов, и, будем надеяться, мы никогда больше не увидим ничего подобного.
Где и когда будут производить вакцину «Спутник V»?
По словам министра промышленности Дениса Мантурова [], серийный выпуск вакцины (помимо производства на базе НИИ им. Гамалеи) планируется в партнерстве с тремя российскими фармацевтическими компаниями — «Генериум», «Р-Фарм» и «Биннофарм». Старт ожидается в сентябре. По предварительным оценкам, за счет работы на контрактных площадках объем производства может достичь нескольких сотен тысяч доз вакцины в месяц с последующим увеличением до нескольких миллионов к началу 2021 года. Финальный объем будет зависеть от потребностей системы здравоохранения.
Компания «Р-Фарм» не только стала одной из первых на фармрынке России, кто включился в борьбу с коронавирусной инфекцией, но и уже успела приобрести разработку оксфордской вакцины от COVID-19. Компания прокомментировала свои планы «РБК Стиль»: «Согласно достигнутым договоренностям, группа компаний «Р-Фарм» займется контрактным производством вакцины «Спутник V». В настоящее время уже производится субстанция, идет процесс разработки промышленных регламентов, проходят валидационные серии. Первые коммерческие партии будут выпущены в октябре, к концу года мы развернем полномасштабное производство. Кроме этого, группа компаний «Р-Фарм» и английская биофармацевтическая компания AstraZeneca заключили соглашение о производстве и коммерциализации в России AZD1222 — вакцины от коронавируса, созданной в лаборатории Оксфорда. Также предполагается экспорт на международные рынки Ближнего Востока, СНГ, Балканского региона, стран Северной Африки».
8 сентября компания AstraZeneca объявила [] о приостановке III фазы клинических испытаний вакцины AZD1222 в связи со случаем поперечного миелита (воспаления одного или нескольких отделов спинного мозга) у одного из добровольцев. Разработчики выясняют, стало ли это побочным эффектом прививки или нет. По словам представителя AstraZeneca [], приостановка испытаний в случае непредвиденного серьезного ухудшения состояния здоровья добровольцев — рутинная процедура во время клинических испытаний, необходимая для обеспечения безопасности участников.
К началу октября в России может быть зарегистрирована еще одна вакцина от COVID-19 — «ЭпиВакКорона», разработанная ГНЦ вирусологии и биотехнологии «Вектор» Роспотребнадзора России. II этап клинических испытаний завершен, серьезных побочных эффектов не выявлено [].
Кто еще в списке?
Еще одним перспективным вариантом, уже дошедшим до стадии клинических испытаний, является цельновирионная вакцина, над которой работает Научный центр исследований и разработки иммунобиологических препаратов имени М.П. Чумакова (Москва).
Цельновирионная вакцина — это настоящий «дикий» вирус, который убивают химическим путем, блокируя его способность к репликации, но не повреждая его специфические белки. С одной стороны, такую вакцину достаточно легко создать и легко модифицировать вместе с мутациями самого вируса. Кроме того, такая вакцина по своему составу гораздо ближе к настоящему вирусу и обычно создает сильный иммунный ответ.
С другой стороны, вакцины на основе мертвых вирусов всегда вызывают опасения с точки зрения безопасности. Ведь фактически «порча» механизма воспроизводства вируса производится химическим путем, что не гарантирует 100%-ной надежности. Кроме того, для наработки вирусов все равно надо кого-то использовать — например, недешевых лабораторных животных, которых сознательно заражают COVID-19.
Добавим, что в списке ВОЗ присутствуют еще несколько российских вакцин, находящихся на доклинической стадии испытаний. В частности, это разработка Санкт-Петербургского научно-исследовательского института вакцин и сывороток, в которой инновационно используется плазмид на основе вирусного генома.
Плазмид — это полностью искусственная оболочка с вирусной ДНК/РНК внутри. Сам по себе плазмид, в отличие от вируса, не способен проникнуть в клетку или делает это крайне плохо. Поэтому для введения плазмидов используют различные физические способы, нарушающие целостность мембран человеческих клеток, например инъекция массивом микроигл, ультразвук или электрический ток.
Поскольку плазмиды в своем начальном состоянии инертны и долго сохраняются в организме, такую вакцинацию можно регулировать с помощью повторного применения дестабилизирующих клеточные мембраны факторов и контролировать титр антител. Кроме того, генный материал вируса из плазмида попадает в клетки, поэтому они тоже становятся «бесплатными фабриками» вирусного белка, как и в варианте с вирусом-вектором.
Похожий подход используется и в вакцине, разработку которой ведет Московский государственный университет имени М.В. Ломоносова. В ней в качестве плазмида выступает модифицированный вирус табачной мозаики, в дикой природе поражающий растения табака. Для человека такой вирус совершенно безопасен, но его хорошая изученность позволяет использовать его в качестве удобного носителя для вирусной информации коронавируса COVID-19. Да и нарабатывать будущие плазмиды в листьях растений табака куда проще, чем в организме лабораторных мышей.
Как видим, спектр разрабатываемых и испытываемых сегодня в России вакцин никак не вяжется с утверждениями о том, что наша страна якобы «утратила» научный потенциал, необходимый для их разработки. Наоборот — сегодня Россия находится на переднем крае борьбы с коронавирусом, а отечественные вакцины опережают разработки зарубежных конкурентов и могут обеспечить для всего мира гарантированную защиту от нового опасного заболевания.
Впереди планеты всей

Принятые в период пандемии меры по защите населения оказались даже эффективнее против других заболеваний.
Вакцина создана специалистами ИЭМ и организации «Биокад».
«Определенные моменты, касающиеся этого препарата для вакцинации, сегодня относятся к ноу-хау, поэтому я не имею права вдаваться в подробности. Но в реальном времени идут доклинические испытания, это никакой не секрет», — сообщил «РИА Новости» эксперт.
Дмитриев добавил, что эти исследования завершатся в скором времени.
Глава Роспотребнадзора Анна Попова 05 декабря 2020 года назвала в числе создаваемых вакцин в РФ объединенный препарат против гриппозной патологии и ковид-19 на базе вируса кори. Центр «Вектор» разработал вакцину в октябре.
Подозреваете ли у себя коронавирус на данный момент?
Да, все признаки имеются 29.85%
Да, и это уже точно 10.39%
Да, но больше склоняюсь к тому, что это обычная простуда 31.27%
Нет 28.49%
Проголосовало: 3658
Как заявил гендиректор центра, в «Векторе» выполнили комплексное испытание коинфицирования вирусным гриппом и ковид-19. И оно показало, что одновременная заболеваемость в разы повышает тяжесть и смертность именно от гриппа.
Позже, 08 декабря 2020 года, в департаменте Министерства здравоохранения РФ рассказали, что сегодня ведется разработка еще 24 препаратов для массовой вакцинации от коронавирусной инфекции, не считая прошедших обязательную регистрацию.
Читайте далее:
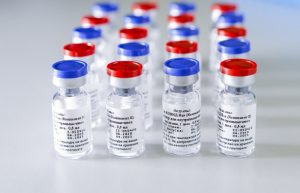
Между вакцинами от коронавируса началась политическая конкуренция
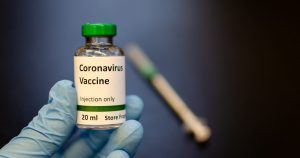
У добровольцев, привитых австралийской вакциной, выявлены положительные тесты на ВИЧ: разработка вакцины остановлена
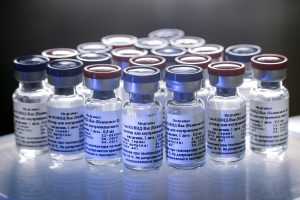
В России подтвердили эффективность всех российских вакцин от коронавируса
Мне нравитсяНе нравится
Фильтр:
Все
Ждет ответа
СортировкаПросмотрыОтветовГолоса
Можно ли носить контактные линзы при коронавирусе?
Дмитрий 1 месяц
7328 просм.
1 ответ.
голос.
Можно ли заразиться через открытую рану?
Мария 1 месяц
6163 просм.
4 ответ.
1 голос.
Переносят ли комары коронавирус?
Фёдор Исаев 1 месяц
6060 просм.
6 ответ.
-4 голос.
Почему требуется так много времени для разработки вакцины?
Прежде чем вакцина станет общедоступной, исследователи должны доказать государственным регулирующим органам, что она эффективна и безопасна в использовании. Это требует времени. Как и все лекарства, после того, как вакцины были испытаны на экспериментальных животных, они проходят три фазы тестирования на людях:
- Несколько здоровых добровольцев получают вакцину. Тестируется безопасность и определяется необходимое количество вакцины.
- Разработка дозировки и проверка безопасности на выборке из большего числа людей.
- Сравнение результатов, полученных от выборки вакцинированных испытуемых с выборкой из людей, зараженных короновирусом. Эта фаза является наиболее трудоемким этапом тестирования, поскольку исследователи должны ждать, пока достаточное количество участников не подвергнется воздействию вируса естественным путем.
Эти условия могут быть рассмотрены в течение нескольких месяцев, если все пойдет хорошо. Создание производственных мощностей также требует времени. Вакцины для клинических испытаний, как правило, производятся небольшими партиями на экспериментальных установках. Но поскольку очень немногие кандидатные вакцины успешно проходят клинические испытания производители, очевидно, неохотно вкладывают средства в крупномасштабное производство, пока не узнают, что вакцина будет работать. Это добавляет дополнительные временные ограничения к процессу разработки вакцины.
Вакцина от коронавируса в Германии
Главные игроки биофармацевтики в Европе расположены в Германии. Это BioNTech и CureVac.Обе они специализируются на исследованиях матричных РНК-терапий. Их метод основан на выключении синтеза белка, участвующего в развитии ОРВИ. Первая компания начнет испытания на людях уже в апреле этого года. CureVac – только к середине лета.
Компания CureVac также сообщила о наращивании производственных мощностей, чтобы изготавливать «миллиарды вакцин» для потребления по всему миру.
Скандал с администрацией США
В середине марта 2020 года произошел скандал, связанный с производством вакцин. Причиной его стала попытка администрации президента США Дональда Трампа переманить к себе исследовательский состав компании, и купить разработки за 1 млрд долларов. В переговорах участвовал и лично президент. При этом, использование вакцины предполагалось только для жителей США. Такое положение дел возмутило жителей Германии и руководство страны. Претензии о попытке вывезти технологии американцами будут подняты на саммите ООН.
Какие могут быть побочные эффекты у вакцины «Спутник V», какие риски и противопоказания?
Согласно методическим рекомендациям Министерства Здравоохранения РФ [], вакцина предназначена для людей 18–65 лет
С осторожностью следует назначать вакцинацию пациентам с хроническими заболеваниями печени и почек, выраженными нарушениями функции эндокринной системы (сахарный диабет), при тяжелых заболеваниях системы кроветворения, эпилепсии, инсультах и других заболеваниях центральной нервной системы, заболеваниях сердечно-сосудистой системы (инфаркт миокарда в анамнезе, миокардит, эндокардит, перикардит, ишемическая болезнь сердца), первичных и вторичных иммунодефицитах, аутоиммунных заболеваниях, заболеваниях легких, метаболическом синдроме, аллергических реакциях, атопии, экземе
Противопоказания для введения первого компонента:
- гиперчувствительность к какому-либо компоненту вакцины;
- тяжелые аллергические реакции в анамнезе;
- острые инфекционные и неинфекционные заболевания, обострения хронических заболеваний (вакцинацию проводят через 2–4 недели после выздоровления или ремиссии);
- при нетяжелых ОРВИ, острых инфекционных заболеваниях желудочно-кишечного тракта вакцинацию проводят после нормализации температуры тела (если температура тела выше 37 °C, вакцинацию откладывают);
- беременность и период грудного вскармливания;
- возраст до 18 лет и старше 60 лет (в связи с отсутствием данных об эффективности и безопасности).
Противопоказания для введения второго компонента:
тяжелые поствакцинальные осложнения на введение первого компонента.
По результатам отчета, опубликованного в журнале The Lancet, на этапе клинических исследований были зафиксированы следующие побочные эффекты: боль в месте введения (58%), гипертермия (50%), головная боль (42%), астения (28%), боль в мышцах и суставах (24%). Острых непредсказуемых реакций не выявлено.
Однако из-за крайне небольшого числа испытуемых (официально данные опубликованы только по 76 добровольцам) есть основания полагать, что разработчики и исследователи могли пока просто не выявить редкие и более тяжелые реакции. О безопасности (или опасности) вакцины скажут результаты III фазы клинических исследований на более обширной выборке.
Какие виды вакцин существуют?
Все вакцины нацелены на достижение одной и той же цели: подвергание иммунной системы организма воздействию белков, углеводных фрагментов или антигенов, обнаруживаемых вирусом или другим патогеном. Если все пойдет по плану, «ячейки памяти» в иммунной системе запомнят их. Если вакцинированный человек впоследствии подвергается действию вируса, клетки иммунной системе позволяют быстро реагировать, подавляя развитие заболевания.
В производстве некоторых вакцин, например вакцин против кори и полиомиелита, используется весь вирус, который был либо убит, либо поврежден, чтобы больше не вызывать заболевание. Но поскольку целый вирус предлагает много антигенов иммунной системе — и из-за небольшого риска того, что живой вирус снова может стать патогенным, — много вещей могут пойти не так. Таким образом, вакцины на основе целого вируса нуждаются в тщательном тестировании на безопасность, и этот процесс может занять годы.
Более экспериментальные вакцины также находятся в разработке. Они доставляют не сам антиген, а генетический материал, который его кодирует, обычно инкапсулированный в жировую мембрану. Он проникает в клетки организма и заставляет их самостоятельно вырабатывать соответствующий белок, чтобы вызвать иммунный ответ. Такие вакцины можно было бы создавать быстрее, потому что генетический материал легче производить в массе, чем белки. Но РНК и ДНК вакцины настолько новы, что ни одна из них еще не была одобрена для использования.