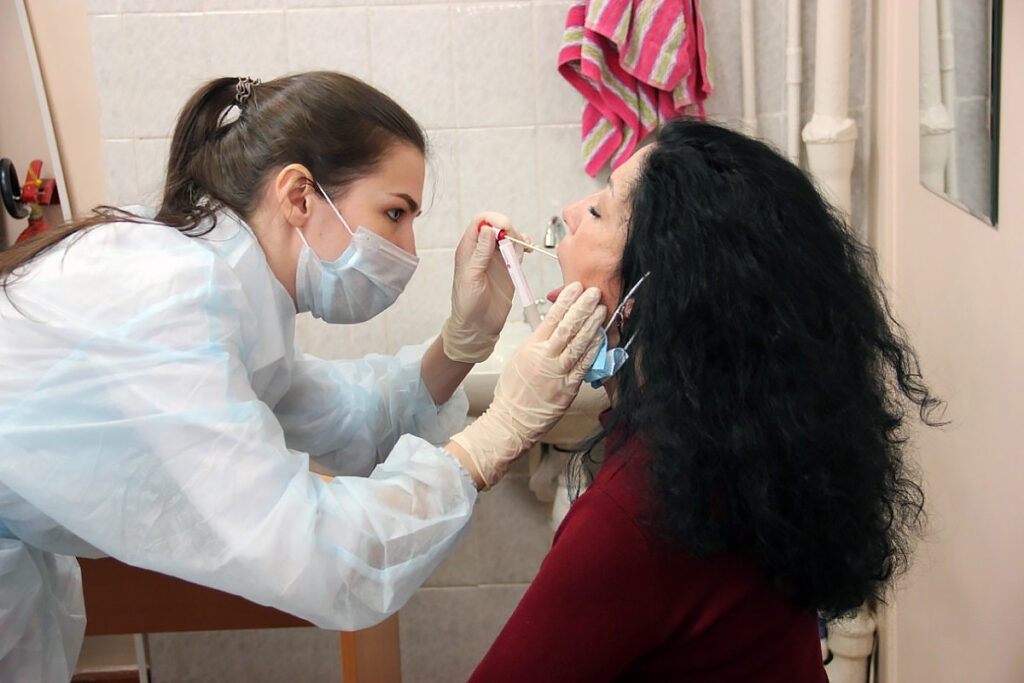Насколько точен анализ на антитела к коронавирусу и как его расшифровать
Содержание:
«Точность ниже, чем у лабораторных тестов»
 — Использовать тесты на антитела для диагностики коронавируса нельзя, — заявляет директор научно-клинического центра прецизионной и регенеративной медицины КФУ Альберт Ризванов. — Их можно использовать только для того, чтобы ответить на вопрос о том, переболел человек ранее или нет, и выработались ли у него антитела. В целом у экспресс-тестов точность ниже, чем у лабораторных. В отличие от последних, они могут сказать только «да» или «нет», то есть, они не могут определить, к примеру, уровень антител. Вообще антитела, особенно на ранних этапах, детектируются не у всех пациентов, следовательно, экспресс-тесты нельзя использовать как диагностику.
— Использовать тесты на антитела для диагностики коронавируса нельзя, — заявляет директор научно-клинического центра прецизионной и регенеративной медицины КФУ Альберт Ризванов. — Их можно использовать только для того, чтобы ответить на вопрос о том, переболел человек ранее или нет, и выработались ли у него антитела. В целом у экспресс-тестов точность ниже, чем у лабораторных. В отличие от последних, они могут сказать только «да» или «нет», то есть, они не могут определить, к примеру, уровень антител. Вообще антитела, особенно на ранних этапах, детектируются не у всех пациентов, следовательно, экспресс-тесты нельзя использовать как диагностику.
Аналогичную позицию озвучивает заместитель премьер-министра РТ Лейла Фазлеева. В беседе с «Реальным временем» вице-премьер заявила, что для подтверждения наличия или отсутствия ковида необходимо пройти лабораторную диагностику, поскольку «экспресс-тесты являются скрининговыми и их результаты не должны использоваться в качестве единственного основания для подтверждения статуса инфекции».
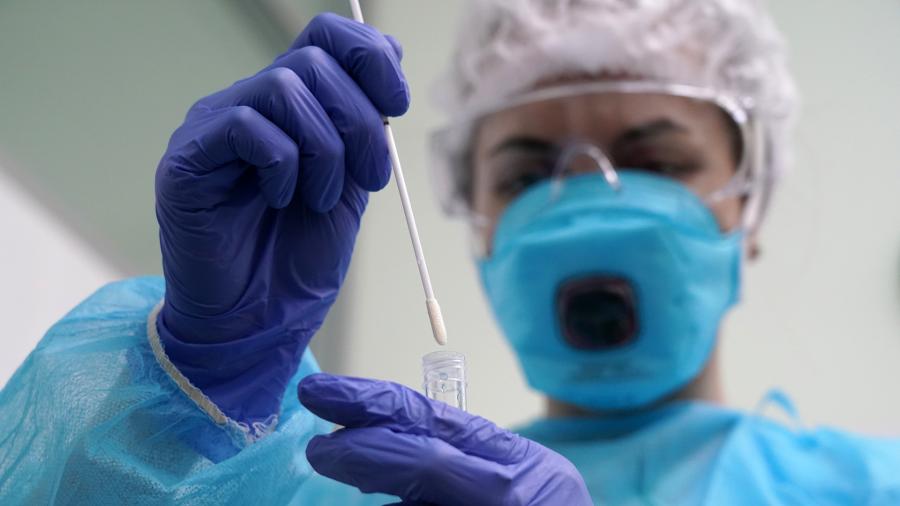
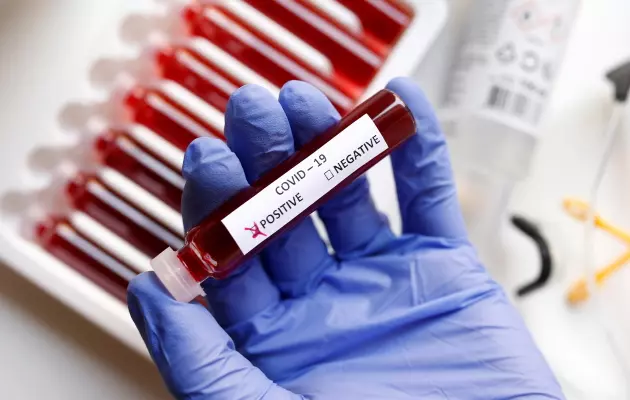
Как пояснил Альберт Ризванов, экспресс-тесты определяют антитела IgM (вырабатываются в самом начале и указывают на активную фазу инфекции или же на то, что человек переболел совсем недавно) или IgG («взрослые» антитела, которые появляются к концу болезни). Само тестирование проходит по следующему алгоритму: берется капля крови, капается в специальное окошко на тест-полоске, а сверху наносится рабочий раствор. Результат готов уже через 8—10 минут. Одна полоска должна проявляться всегда — это значит, что тест сработал, две других полоски показывают антитела M и G.
Точность разных ПЦР-тест-систем
После попадания образцов в лабораторию правильность диагноза будет зависеть во многом от тест-системы, которую там используют. На сегодняшний день помимо двух тест-систем, разработанных еще в январе в ГНЦВБ «Вектор», зарегистрировано 8 ПЦР-тест систем []:
- АмплиТест SARS-CoV-2; разработан ФГБУ «Центр стратегического планирования» (ЦСП) Минздрава РФ, Москва;
- АмплиСенс CoVs-Bat-FL (ЦНИИ Эпидемиологии Роспотребнадзора, Москва);
- Поливир SARS-CoV-2 (ООО «НПФ «Литех», Москва совместно с ФМБА и НИЦЭМ им. Гамалеи);
- РеалБест РНК SARS-CoV-2 (АО «Вектор-Бест», Новосибирск, Кольцово);
- набор реагентов для выявления РНК коронавирусов SARS-CoV-2 и подобных SARS-CoV (ООО «ДНК-Технология-ТС», Москва);
- набор реагентов для выявления РНК коронавируса SARS-CoV-2 (ФГБУ «48 ЦНИИ» Минобороны России);
- SBT-DX-SARS-CoV-2 (ООО «Система-БиоТех»);
- набор ООО «МедипалТех» из Дубны (производителем указано ООО «Амплитек»).
Из них системы «Вектора» и «Вектор-беста» (последняя через сеть лабораторий «Инвитро» []) используются для исследования проб от государственных медицинских учреждений, поликлиник и больниц. Здесь хочется отметить, что система «Вектора» не содержит в своем составе внутреннего контрольного образца, который должен добавляться во все пробы для контроля правильности выделения РНК и реакции обратной транскрипции []. Отсутствие такого контроля может также потенциально приводить к некоторому количеству ложноотрицательных результатов. Хорошая новость заключается в том, что остальные зарегистрированные тест-системы имеют в своем составе внутренний контроль, а также, по-видимому, обладают более высокой чувствительностью, т.е. дают меньше ложноотрицательных результатов.
Что касается частных клиник, то компании «Хеликс» [] и «Гемотест» [] заявляют, что они используют систему ГНЦВБ «Вектор», в то время как CMD и «Ситилаб » используют более современные системы ЦНИИ Эпидемиологии и ДНК-технологии, соответственно [,
Таким образом, в городах, где представлены сетевые лаборатории, есть возможность сдать анализ частным образом и надеяться на точность проведения процедуры. В первые дни появления симптоматики точность будет выше.
Почему пока рано говорить, что антитела служат надежной защитой от коронавируса
Сейчас органы здравоохранения, Минобороны и правительство США сотрудничают с представителями научных кругов и медработников, чтобы установить, действительно ли положительные тесты на антитела показывают наличие иммунитета к SARS-CoV-2. Им предстоит оценить уровень антител, необходимых для защиты от повторного заражения, длительность этой защиты, факторы, связанные с выработкой антител, и многое другое.
Хотя исследования на животных показывают защиту в краткосрочной перспективе, демонстрация долгосрочной защиты у людей потребует будущих исследований. Следовательно, до получения дополнительных данных присутствие антител нельзя отождествлять с иммунитетом человека от инфекции SARS-CoV-2.
Плюс ко всему некоторые тесты могут показать перекрестную реактивность с другими коронавирусами, например теми, что вызывают простуду. Это может привести к ложноположительным результатам теста. А некоторые люди могут не выработать обнаруживаемые антитела даже после коронавирусной инфекции.
В других случаях возможно, что уровни антител могут со временем снижаться до неопределяемых уровней (антитела IgM и IgG не присутствуют на ранних стадиях инфекции). Таким образом, результаты тестов на наличие антител не могут уверенно свидетельствовать, что человек перенес или все еще болеет коронавирусной инфекцией.
Background
Serologic assays for SARS-CoV-2, now broadly available, can play an important role in understanding the virus’s epidemiology in the general population and identifying groups at higher risk for infection. Unlike direct detection methods such as viral nucleic acid amplification or antigen detection tests that can detect acutely infected persons, antibody tests help determine whether the individual being tested was previously infected—even if that person never showed symptoms. Serologic tests detect resolving or past SARS-CoV-2 virus infection indirectly by measuring the person’s humoral immune response to the virus. Therefore, serologic assays do not typically replace direct detection methods as the primary tool for diagnosing an active SARS-CoV-2 infection, but they do have several important applications in monitoring and responding to the COVID-19 pandemic.
Although serologic tests should not be used at this time to determine if an individual is immune, these tests can help determine the proportion of a population previously infected with SARS-CoV-2 and provide information about populations that may be immune and potentially protected. Thus, demographic and geographic patterns of serologic test results can help determine which communities may have experienced a higher infection rate and therefore may have a higher proportion of the population with some degree of immunity, at least temporarily. In some instances, serologic test results may assist with identifying persons potentially infected with SARS-CoV-2 and determining who may qualify to donate blood that can be used to manufacture convalescent plasmaexternal icon as a possible treatment for those who are seriously ill from COVID-19.
Development of Antibodies and Immunity
Nearly all immune-competent individuals will develop an immune response following SARS-CoV-2 infection. Like infections with other pathogens, SARS-CoV-2 infection elicits development of IgM and IgG antibodies, which are the most useful for assessing antibody response because little is known about IgA response in the blood.
Antibodies in some persons can be detected within the first week of illness onset. In SARS-CoV-2 infections, IgM and IgG antibodies can arise nearly simultaneously in serum within 2 to 3 weeks after illness onset. Thus, detection of IgM without IgG is uncommon. How long IgM and IgG antibodies remain detectable following infection is not known. It is also important to note that some persons do not develop detectable IgG or IgM antibodies following infection. Thus, the absence of detectable IgM or IgG antibodies does not necessarily rule out that they could have previously been infected.
In addition, development of neutralizing antibodies can also be assessed. Neutralizing antibodies inhibit viral replication in vitro, and as with many infectious diseases, their presence correlates with immunity to future infection, at least temporarily.
Recurrence of COVID-19 illness appears to be very uncommon, suggesting that the presence of antibodies could indicate at least short-term immunity to infection with SARS-CoV-2. Consistent with this observation, experimental primary infection in primates and subsequent development of antibodies resulted in protection from reinfection after the primates were rechallenged. Additionally, antibody development in humans correlates with a marked decrease in viral load in the respiratory tract. Taken together, these observations suggest that the presence of antibodies may decrease a person’s infectiousness and offer some level of protection from reinfection. However, it remains uncertain to what degree and for how long individuals with antibodies (neutralizing or total) are protected against reinfection with SARS-CoV-2 or what concentration of antibodies may be needed to provide such protection.
Accuracy of antibody tests
Accuracy is a measure of how well the tests detect previous SARS-CoV-2 infections, and not a direct measure of immunity to future infections. The accuracy of SARS-CoV-2 antibody tests is measured by comparing the test results with a gold standard: usually viral RNA detection by PCR testing at the time of symptoms. A limitation of this approach is the sensitivity in PCR testing (which may be as low as 70%).
A Cochrane review of SARS-CoV-2 antibody testing included 57 publications on 54 cohort studies with 15 976 samples, of which 8526 were from cases of confirmed SARS-CoV-2 infection. Measures of diagnostic accuracy varied depending on the timing of the tests (). The maximum sensitivity for combined IgG or IgM tests was 96% at days 22-35 after symptom onset. For IgG alone the maximum sensitivity was 88.2% at days 15-21 after symptom onset. Summary specificities were provided in 35 out of 54 studies and exceeded 98% for all types of antibody test.
Table 1
Sensitivity and specificity by time since symptom onset6
View this table:
Наличие антител в крови означает иммунитет к коронавирусу?

На этот вопрос пока сложно ответить. Почти у всех иммунокомпетентных людей (так называются клетки иммунной системы организма, способные специфически взаимодействовать с антигеном) развивается иммунный ответ после COVID-19. Подобно другим инфекциям, SARS-CoV-2 вызывает выработку антител IgM и IgG, которые являются наиболее полезными для оценки иммунного ответа (сейчас мало что известно об «ответе» IgA в крови).
В случае с SARS-CoV-2 антитела IgM и IgG возникают почти одновременно в сыворотке крови в течение 2-3 недель после начала заболевания. Таким образом, обнаружение IgM без IgG является редкостью. Как долго антитела IgM и IgG остаются обнаруживаемыми после инфекции, неизвестно.
ЦКЗ также изучил, коррелирует ли развитие нейтрализующих антител с иммунитетом к коронавирусу. По мнению исследователей, рецидив заболевания COVID-19, по-видимому, является весьма редким событием. Это позволяет предположить, что присутствие антител может обеспечить по меньшей мере кратковременный иммунитет к коронавирусной инфекции. В частности, у приматов, переболевших коронавирусом, появлялась защита от повторного заражения. Кроме того, развитие антител у человека коррелирует с заметным снижением вирусной нагрузки в дыхательных путях.
Говоря более простыми словами, наличие антител может снизить заразность человека и обеспечить некоторый уровень защиты от повторного заражения. Однако точные данные отсутствуют, и исследователи все еще не уверены, защищены ли люди с антителами (нейтрализующими или суммарными) от повторной инфекции SARS-CoV-2 и какая концентрация антител необходима для защиты.